„Mokslo sriubos“ žurnalistė Elizabet Beržanskytė
Pirmoji vakcina
Raupai buvo pandemija, dėl kurios vien XX amžiuje visame pasaulyje mirė daugiau nei 300 mln. žmonių. Ši liga egzistavo daugiau nei 3000 metų, o pirmieji užrašai apie panašaus užkrato egzistavimą buvo randami jau netgi IV a. Kinijoje bei VII a. Indijoje. Ir tada, kai jau niekas nieko nebesitikėjo, 1796 m. įvyko vienas svarbiausių atradimų mokslo pasaulyje – buvo atrasti skiepai. Šio atradimo tėvu laikomas anglų medikas Edward Jenner. Jis pastebėjo, jog pienininkės, kurios užsikrečia karvių raupais, žmogiškaisiais raupais vėliau nebeserga. Mokslininkas spėjo, jog, greičiausiai, karvių liga kažkokiu būdu leidžia apsisaugoti nuo užsikrėtimo vėliau šios ligos žmogiškąja versija. Siekdamas patikrinti savo teoriją, jis paskiepijo savo sodininko sūnų medžiaga paimta nuo vienos iš karvių raupais užsikrėtusios melžėjos žaizdos. Po 9 mėnesių E. Jenner kelis kartus bandė užkrėsti berniuką žmogiškuosius raupus sukeliančiu virusu, bet vaikas nei karto nesusirgo. 1798 m. buvo sukurta pirmoji vakcina nuo raupų, o 1980 metų gegužės 8 d. 33-oji Pasaulio sveikatos asamblėja paskelbė pasaulį visiškai pasveikus nuo raupų.
Ir nors primityvūs imunizacijos metodai (pvz.: budistų vienuoliai gerdavo gyvačių nuodus, siekdami įgyti jiems imunitetą ir ateityje lengviau išgyventi įkandimus) buvo taikomi jau nuo senų laikų, šis E. Jenner atradimas tapo dideliu postūmiu medicinos mokslų srityje. Netikėtai išsiaiškinus vieną iš galimų apsisaugojimo nuo užkrečiamų ligų būdų, daugelis mokslininkų nukreipė savo jėgas būtent į šią sferą. Per 1930-uosius metus buvo sukurti skiepai prieš cholerą, tuberkuliozę, difteriją, stabligę, juodligę, vidurių šiltinę ir kai kurias kitas daugelį metų žmones kankinusias ligas.
Naujų skiepų kūrimas žengė koja kojon su naujų laboratorinių metodų atradimais. Tad XX a. buvo dar dosnesnis. Išmokus virusus auginti laboratorijose, pasaulį išvydo skiepai, skirti kovoti su kokliušu, poliomielitu, tymais, kiaulyte, raudonuke.
Pažymėtina, jog tobulėjant vakcinų kūrimo technologijoms, kartu vis labiau buvo vystomas jų patikros ir išleidimo į rinką procesas. Šiais laikais visi nauji rinkoje atsirandantys vaistiniai preparatai, įskaitant ir vakcinas (pvz.: nuo SARS-CoV-2 viruso sukeliamos COVID-19 ligos) po pirminio varianto sukūrimo iki masinio vartojimo turi praeiti ne vieną ir ne du tobulinimo ir patikros etapus. Taip užtikrinamas maksimalus preparato saugumas, efektyvumas ir kokybė.
Vakcinos gyvenimo etapai
Šiais laikais bet kuris medikamentas nuo idėjos iki masinio vartojimo paprastai praeina tris didelius gyvenimo etapus. Pačioje pradžioje yra pagaminami maži vakcinos kiekiai bei vykdomi jų laboratoriniai bandymai. Vienų metu – siekiama nustatyti tinkamiausią formuluotę, kuri išlaikytų vakcinos komponentus stabilius iki pačios vakcinos galiojimo pabaigos, kitų – optimizuojamas preparato gaminimo procesas.
Tolimesnis etapas – preklinikiniai tyrimai. Jis skirtas papildomiems laboratoriniams testams, o taip pat vakcinos veikimo patikrai gyvūnų modeliuose. Pastarųjų eksperimentų pagrindiniai tikslai – nustatyti vakcinos veiksmingumą, saugumą, poveikį vaisingumui ir embriono vystymuisi.
Įvykdžius preklinikinius eksperimentus ir gavus teigiamus rezultatus, yra pereinama prie klinikinių tyrimų. Šių bandymų metu tiriamas vakcinos poveikis žmogui. Jie dažniausiai skirstomi į 3 smulkesnes fazes.
I fazės metu tiriamųjų grupę sudaro 20-100 sveikų savanorių ir yra siekiama atsakyti į kelis svarbius klausimus: ar vakcina iššaukia reikiamą imuninį atsaką, ar ji saugi toliau vykdyti didesnės apimties tyrimus, kurios preparato dozės galėtų būti tinkamiausios naudojimui? Dar tikslesnės dozės ir reikiamas jų skaičius nustatomas klinikinių tyrimų II fazės metu. Šio etapo tiriamųjų grupę sudaro keli šimtai skirtingos sveikatos būklės ir skirtingų demografinių grupių savanoriai. Paprastai vakcina paskiepyti žmonės yra lyginami su žmonėmis iš kontrolinės grupės, į kurią įeina jau seniau patvirtintu arba placebo preparatu paskiepyti asmenys. Svarbu ir tai, kad būtent klinikinių tyrimų II fazės eigoje yra stebimi dažniausiai pasitaikantys šalutiniai poveikiai.
III-ioje klinikinių tyrimų fazėje savanoriai skaičiuojami tūkstančiais. Lyginant paskiepytų eksperimentine vakcina ir žmonių iš kontrolinės grupės duomenis, yra tikrinamas naujo skiepo efektyvumas (apsaugant nuo infekcijos). Taip pat šio etapo metu nustatomi retesni šalutiniai poveikiai.
Klinikinių tyrimų eigoje išrinkus tinkamiausią vakcinos kandidatą, reikia gerai apgalvoti ir optimizuoti jo pramoninį gaminimą. Labai svarbu, kad dideliais kiekiais gaminami, fasuojami ir transportuojami vakcinų gamybai skirti reagentai išlaikytų tiek kokybę, tiek savybes, o galiausiai visos masiškai pagamintos vakcinos būtų identiškos.
Tolimesnis žingsnis po vakcinos sukūrimo ir gamybos sąlygų numatymo – preparato patvirtinimas. Europoje visų ankstesnių vakcinos gaminimo etapų duomenys pirmiausiai yra perduodami Europos vaistų agentūrai (angl. The European Medicines Agency (EMA)), kuri pateikia rekomendaciją, ar vaistą reikėtų pristatyti rinkai, ar ne. Vėliau Europos Komisija turi išduoti vaisto įregistravimo pažymėjimą ir tik tada preparatas gali būti gaminamas bei platinamas Europos Sąjungos šalyse. Po šio patvirtinimo kiekvienos šalies valdžia svarsto galimybę šia vakcina skiepyti savo piliečius bei nustato vakcinacijos politiką.
Svarbu ir tai, kad net ir po patvirtinimo vakcina ir toliau yra tikrinama, stebimi galimi šalutiniai poveikiai. Tai kartais įvardijama kaip klinikinių tyrimų IV-oji fazė.
Kaip taip nutiko, kad vakcinų nuo COVID-19 sulaukėme taip greitai?
O dabar, išsiaiškinus, kodėl skiepai mums yra svarbūs, kaip jie išsaugojo daugelio žmonių gyvybes, ir kaip tobulėjo jų kūrimo bei patikros procesas, sugrįžkime į šių dienų aktualijas. Truputėlį pakrutinkime skiepų nuo COVID-19 temą, o tiksliau, vieną iš daugiausiai diskusijų keliančių šios temos aspektų – skiepo sukūrimą. ,,Kodėl skiepai atsirado taip greitai? Ar jie pakankamai patikrinti? Ar patikimi? Ar tikrai saugūs?“ – šie ir panašūs klausimai, manau, kyla dažnam, besvarstančiam skiepijimosi nuo COVID-19 ligos, galimybę. Tačiau, kur yra ieškoma atsakymų į šiuos klausimus? Ar išvis ieškoma? Pamėginkime panagrinėti, ką šia tema sako mokslinė literatūra.
Taigi, pirmiausiai, vienas svarbiausių dalykų, kuriuos norėtųsi paminėti – trumpesnis vakcinų ir kitų medicininių preparatų patekimas į rinką tikrai nereiškia, kad jie yra nepatikrinti ar pavojingi. Įprastai vakcinų sukūrimo procesas trunka 5-10 metų. Visgi didelių pandemijų metu yra imamasi papildomų priemonių, kurių pagalba galima būtų per trumpesnį laiką žmonėms pateikti būdą išgyti ar apsisaugoti nuo tam tikros ligos.
Štai pirmoji (laboratorinė) vakcinos kūrimo fazė dažnai gali būti paspartinama jau iš anksto turint žinių apie panašiai veikiančius skiepus bei patogeną prieš kurį kovojama. Nesunku numanyti, kad tik prasidėjus COVID-19 pandemijai visos pasaulio laboratorijos sugužėjo ir ėmėsi panašaus tikslo – kuo daugiau išsiaiškinti apie sparčiai plintančią ligą ir ją sukeliantį virusą. Tad, pradėjus vakcinų kūrimą, žinių apie SARS-CoV-2 turėjome jau tikrai nemažai, o tai leido tiksliau suplanuoti pirminius eksperimentus bei sutaupyti brangaus laiko.
Taip pat, kalbant apie greitą vakcinų išleidimą, norėtųsi paneigti daug kur sklandantį mitą apie tai, jog siekiant kuo greičiau rinkai pateikti vakcinas nuo COVID-19, buvo trumpinami jų kūrimo/patikros etapai. Čia pravartu pažvelgti į įprasto vaistinio preparato kūrimo/patikros fazių laiko juostą. Net ir iš pirmo žvilgsnio joje nesunkiai galima pastebėti, jog visi etapai yra vykdomi su pertraukomis.
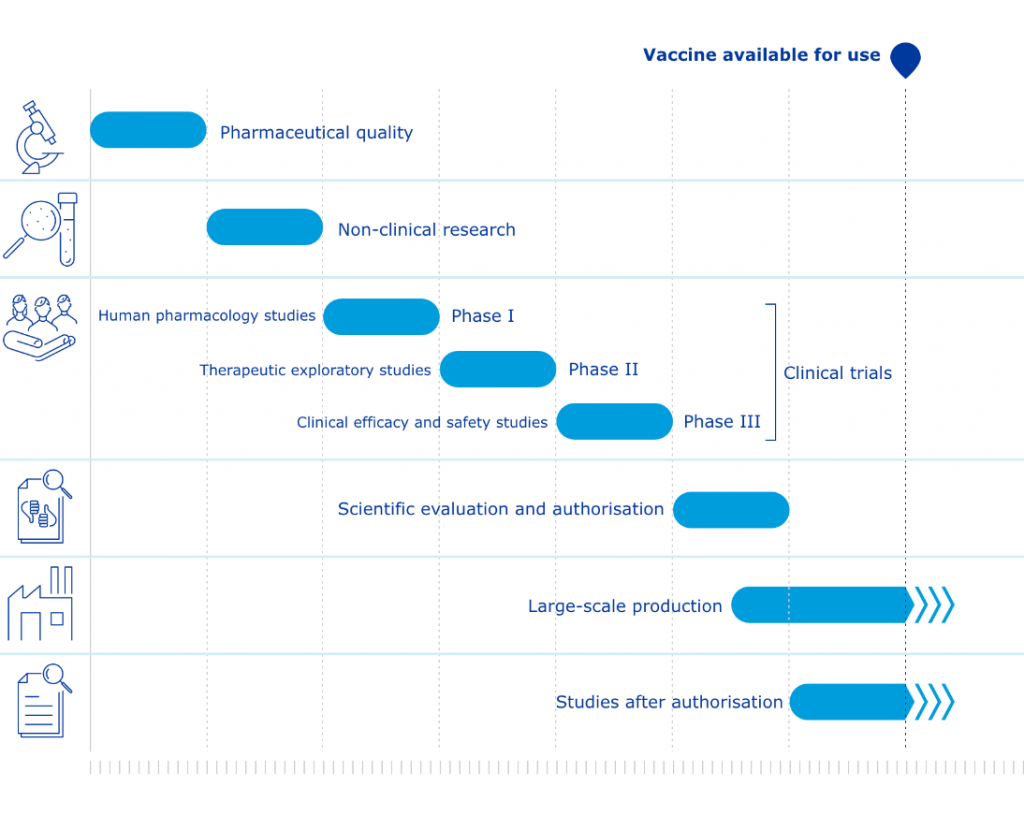
Kalbant apie vakcinos nuo COVID-19 kūrimo procesą, matoma, jog jis tikrai nebuvo sutrumpintas kažkurio vieno ar kelių etapų sąskaita. Anaiptol, jį sudarė visi tie patys etapai (kaip ir įprastai) tik jie laike buvo daug labiau suspausti, o klinikinių tyrimų fazės buvo pereinančios iš vienos į kitą, vietoje to, kad kiekviena jų būtų pradėta nuo nulio.

Pažymėtina, jog kadangi klinikiniai tyrimai paprastai trunka ilgiausiai iš visų vakcinos gamybos/patikros etapų, pandeminėmis sąlygomis, kuomet nėra laiko laukti, kai kada klinikinių tyrimų III fazės vykdymo eigoje Europos vaistų agentūrai pateikus rezultatus, kurie akivaizdžiai įrodo žymiai didesnę vakcinos naudą nei galimus šalutinius poveikius, vaistinis preparatas gali būti išimties tvarka patvirtinamas (angl. conditional marketing authorisation) anksčiau, dar galutinai nepasibaigus tyrimams. Visgi šis leidimas galioja tik metus, o siekiant jį pratęsti ar pervesti į nuolatinį, paraiškos EMA tvirtinimui teikėjas privalo toliau vykdyti papildomus tyrimus ir paskiepytų asmenų stebėjimą. Nauji rezultatai turi nuolat būti teikiami agentūrai, siekiant įrodyti, jog preparato nauda vis dar ženkliai nusveria trūkumus. Svarbu paminėti, jog paraiškos teikėjui neįvykdžius įsipareigojimų ar pristačius reikalavimų neatitinkančius duomenis, EMA sąlyginis leidimas vakcinai gali būti panaikinamas arba sustabdomas.
Dar vienas labai svarbus dalykas, kurio dėka šiandien jau turime galimybę skiepytis ir apsisaugoti nuo COVID-19 ligos – didesniu mastu nei įprastai vykdomos mokslinės konsultacijos. Bet kurio išleidžiamo vaistinio preparato kūrimo procesas yra neatsiejamas nuo diskusijų su ateityje produktą tvirtinančios organizacijos (Europoje – EMA) mokslininkų ekspertų komisijomis. Šios pandemijos laikotarpiu EMA ekspertų, į kuriuos galima kreiptis, skaičiai ženkliai padidėjo. Tai leido greičiau ištobulinti vakcinos gamybos ir produkcijos technologijas.
Taip pat reikia nepamiršti ir to, jog vakcinos mūsų nepasiektų be dviejų svarbių procesų: jų sukūrimo/patikros ir jų pramoninės gamybos. Greitinant bendradarbiavimą tarp abiejų procesų atstovų, didėja ir tikimybė greičiau pristatyti skiepus plačiajai visuomenei. Vienos to pavyzdžių būtent ir yra vakcinos nuo koronaviruso sukeliamos ligos – gamintojai dar ankstyvuose skiepų kūrimo stadijose jau pradėjo galvoti ir ruoštis preparato produkcijai dideliais kiekiais. Be to, dalis įmonių pradėjo gaminti vakcinas dar nepasibaigus klinikinių tyrimų fazei, siekiant pasiruošti tam, kad po vakcinos patvirtinimo, jos galėtų būti iš karto naudojamos.
Na ir žinoma, kaip nepaminėjus visų taip mėgiamo biurokratizmo. Paprastai skirtingų popierių tikrinimo etapai yra vieni tų, kurie užima daugiausiai laiko vaistinių preparatų realizavimo kelyje. Į tai, žinoma, yra atsižvelgiama ekstremaliose aplinkybėse. Vienas tų sušvelninimų, kuris buvo atliktas, siekiant pagreitinti vakcinos nuo COVID-19 sukūrimą buvo greitesnis naujų vakcinos gamybos vietų ar jau egzistuojančiose įmonėse – linijų, patvirtinimas. Be to, įprastai 210 dienų trunkantis EMA dokumentų tvirtinimo procesas, atsižvelgiant į vis prastėjančią situaciją buvo sutrumpintas iki 150 dienų. Ir netgi šis laikotarpis galėjo būti dar labiau trumpinamas, kuomet EMA eksperimentų rezultatų peržiūrą pradėdavo paraleliai su dar vykstančiais tyrimais, vietoje to, kad lauktų visų, anksčiau minėtųjų, kūrimo/patikros fazių pabaigos.
Taigi, kaip galima matyti, ekstremalioje situacijoje (pvz.: pandeminėmis sąlygomis), vakcinos realizavimo kelias gali būti trumpinamas, naudojant skirtingas priemones: iš anksto pasiruošus ir sukaupus daug tyrimuose pritaikomos mokslinės informacijos, pasitelkiant didesnius žmogiškuosius išteklius (dėka didesnio finansavimo), trumpinant biurokratinius procesus. Visgi, nors skiepų prieš SARS-CoV-2 sukeliamą ligą kūrimo/patikros procesas ir šiek tiek skyrėsi nuo įprastinio, svarbu nepamiršti, jog joks vaistinis preparatas negali būti patvirtinamas, jei jis neatitinka kokybės, saugumo ir efektyvumo reikalavimų. Tad teigti, jog skiepai nuo COVID-19 yra nesaugūs ar nepatikrinti dažnu atveju nėra pagrindo.
Šaltiniai:
- https://www.bbc.co.uk/history/british/empire_seapower/smallpox_01.shtml
- https://www.cdc.gov/smallpox/history/history.html
- https://www.chop.edu/centers-programs/vaccine-education-center/vaccine-history/developments-by-year
- https://www.ema.europa.eu/en/documents/other/about-us-european-medicines-agency-ema_lt.pdf
- https://www.ema.europa.eu/en/human-regulatory/marketing-authorisation/conditional-marketing-authorisation
- https://www.ema.europa.eu/en/human-regulatory/overview/public-health-threats/coronavirus-disease-covid-19/treatments-vaccines/vaccines-covid-19/covid-19-vaccines-development-evaluation-approval-monitoring
- https://www.fda.gov/vaccines-blood-biologics/development-approval-process-cber/vaccine-development-101
- https://www.historyofvaccines.org/timeline/all
- https://www.immune.org.nz/vaccines/vaccine-development/brief-history-vaccination
- https://www.medicalnewstoday.com/articles/how-did-we-develop-a-covid-19-vaccine-so-quickly#MNT-takeaways
- https://www.nytimes.com/interactive/2020/science/coronavirus-vaccine-tracker.html
- https://www.who.int/news-room/feature-stories/detail/smallpox-vaccines


